PH-Wert: Unterschied zwischen den Versionen
Admin (Diskussion | Beiträge) |
Admin (Diskussion | Beiträge) |
||
| (7 dazwischenliegende Versionen von einem Benutzer werden nicht angezeigt) | |||
| Zeile 9: | Zeile 9: | ||
In der [[Lederherstellung]] und [[Lederpflege]] ist der pH-Wert dahingehend von Bedeutung, dass durch die [[Gerbung]] im Leder grundsätzlich ein saures Milieu mit einem pH-Wert von ca. 4,5 bis 5,5 erzeugt wird. Dieser pH-Wert sorgt mitunter dafür, dass die im Leder gebundenen Fett- und Gerbstoffe gehalten werden. | In der [[Lederherstellung]] und [[Lederpflege]] ist der pH-Wert dahingehend von Bedeutung, dass durch die [[Gerbung]] im Leder grundsätzlich ein saures Milieu mit einem pH-Wert von ca. 4,5 bis 5,5 erzeugt wird. Dieser pH-Wert sorgt mitunter dafür, dass die im Leder gebundenen Fett- und Gerbstoffe gehalten werden. | ||
| − | Mit der Alterung des Leders verschiebt sich das Säure-Basen-Verhältnis | + | Mit der [[Lederschäden|Alterung des Leders]] verschiebt sich das Säure-Basen-Verhältnis ins Alkalische (über pH 7), was das Leder instabil macht. Das Leder dunkelt, wird hart und brüchig. Die Verschiebung erfolgt durch Alter, Luftfeuchtigkeit und Sonne, aber auch durch Schweiß (Haut-, Haarkontakt) bei [[Autoleder|Auto-]] und [[Ledermöbel|Möbelleder]], Schweiß durch Füße in [[Lederschuhe|Schuhen]] (täglich zwischen 100-200 ml), Hände in [[Lederhandschuhe |Handschuhen]] oder "Speckkragen" bei [[Lederbekleidung|Jacken]]). |
| Zeile 20: | Zeile 20: | ||
</p> | </p> | ||
<p align=center> | <p align=center> | ||
| − | ''Typische Schäden durch Haut- und Haarkontakt bei [[Möbelleder]] | + | ''Typische Schäden durch Haut- und Haarkontakt bei [[Möbelleder|Möbelledern]] (Kopfteile und Armlehnen).''<br></p> |
<p> </p> | <p> </p> | ||
| Zeile 31: | Zeile 31: | ||
</p> | </p> | ||
<p align=center> | <p align=center> | ||
| − | ''Auch Lenkräder reagieren mit der Zeit auf Handschweiß. Durch die pH-Verschiebung wird das Leder auch anfälliger für [[Schimmel]] | + | ''Auch [[Lederlenkrad|Lenkräder]] reagieren mit der Zeit auf Handschweiß. Durch die pH-Verschiebung wird das Leder auch anfälliger für [[Schimmel|Schimmelbefall]].''<br></p> |
<p> </p> | <p> </p> | ||
| Zeile 43: | Zeile 43: | ||
</p> | </p> | ||
<p align=center> | <p align=center> | ||
| − | ''Durch Hautkontakt geschädigte Auto-Armlehnen und ein Schaltknauf''<br></p> | + | ''Durch Hautkontakt geschädigte Auto-Armlehnen und ein Schaltknauf.''<br></p> |
<p> </p> | <p> </p> | ||
| + | Ein weiterer Grund sind alkalische [[Lederreiniger|Reiniger]]. Die meisten Haushaltsreiniger sind alkalisch, weil dann problemlos eine gute Reinigungswirkung entsteht. Lederreiniger sollten aber nicht alkalisch sein, was technisch auch möglich ist, aber nicht von allen Herstellern beachtet wird. | ||
| − | + | Auch die Pflegemittel sollten idealerweise den sauren Zustand wiederherstellen bzw. aufrechterhalten. Gerade bei [[Schimmel|Schimmelbefall] an Altledern eignet sich beispielsweise Essigessenz als pH-Regulator zur Entfernung und Vorbeugung vorzüglich. Auch bei der generellen Altlederrestauration ist eine Rücksäuerung ebenso wichtig wie eine [[Lickern|Rückfettung]], um das Leder wieder resistenter gegen Umwelteinflüsse zu machen. | |
| − | + | ||
| − | Auch die Pflegemittel sollten idealerweise den sauren Zustand wiederherstellen bzw. aufrechterhalten. Gerade bei [[Schimmel] | + | |
Gleichwohl gibt es natürlich auch eine Grenze, wieviel Säure ein Leder verträgt. Ein gelegentlich in Bibliotheken zu beobachtender, charakteristischer Säureschaden an [[Bucheinband|Bucheinbänden]] ist etwa der [[Roter Zerfall|Rote Zerfall]], wenn Schwefeldioxid aus der Luft im Leder zu Schwefelsäure reagiert, die den Einband irreparabel zerfrisst. Schwefelsäure ist allerdings auch eine der stärksten Säuren und untertrifft den für Leder maximal verträglichen pH-Wert von 3,5 bei weitem. | Gleichwohl gibt es natürlich auch eine Grenze, wieviel Säure ein Leder verträgt. Ein gelegentlich in Bibliotheken zu beobachtender, charakteristischer Säureschaden an [[Bucheinband|Bucheinbänden]] ist etwa der [[Roter Zerfall|Rote Zerfall]], wenn Schwefeldioxid aus der Luft im Leder zu Schwefelsäure reagiert, die den Einband irreparabel zerfrisst. Schwefelsäure ist allerdings auch eine der stärksten Säuren und untertrifft den für Leder maximal verträglichen pH-Wert von 3,5 bei weitem. | ||
| Zeile 110: | Zeile 109: | ||
|- | |- | ||
| Milch | | Milch | ||
| − | |style="background-color: #339933; text-align: center"| 6,5 | + | |style="background-color: #339933; text-align: center"| 6,5 |
|- | |- | ||
| Wasser (je nach Härte) | | Wasser (je nach Härte) | ||
| Zeile 143: | Zeile 142: | ||
|style="background-color: #0000CC; text-align: center; color: #FFFFFF"| 12,6 | |style="background-color: #0000CC; text-align: center; color: #FFFFFF"| 12,6 | ||
|- | |- | ||
| − | | Natriumhydroxid | + | | Natriumhydroxid, Natronlauge (Ätznatron) |
|style="background-color: #000099; text-align: center; color: #FFFFFF"| 13,5–15 | |style="background-color: #000099; text-align: center; color: #FFFFFF"| 13,5–15 | ||
|} | |} | ||
</center> | </center> | ||
| − | |||
| − | |||
| − | |||
| Zeile 160: | Zeile 156: | ||
| − | < | + | <logoplustext /> |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
Aktuelle Version vom 23. November 2022, 17:43 Uhr
Der pH-Wert von Leder
Der pH-Wert (lat.: potentia Hydrogenii, "Kraft des Wasserstoffs") eines Stoffes bezeichnet in zehnerlogarithmischen Abständen, wie sauer bzw. basisch dieser Stoff ist. Destilliertes Wasser ist mit einem pH-Wert von 7 definiert, so dass - im Vergleich - ein Stoff mit pH-Wert 8 (wie Meerwasser) zehnmal basischer ist und ein Stoff mit pH-Wert 5 (z. B. Kaffee) einhundertmal saurer ist. Cola hat einen pH-Wert von 2 und ist damit hunderttausendmal saurer als destilliertes Wasser.
In der Lederherstellung und Lederpflege ist der pH-Wert dahingehend von Bedeutung, dass durch die Gerbung im Leder grundsätzlich ein saures Milieu mit einem pH-Wert von ca. 4,5 bis 5,5 erzeugt wird. Dieser pH-Wert sorgt mitunter dafür, dass die im Leder gebundenen Fett- und Gerbstoffe gehalten werden.
Mit der Alterung des Leders verschiebt sich das Säure-Basen-Verhältnis ins Alkalische (über pH 7), was das Leder instabil macht. Das Leder dunkelt, wird hart und brüchig. Die Verschiebung erfolgt durch Alter, Luftfeuchtigkeit und Sonne, aber auch durch Schweiß (Haut-, Haarkontakt) bei Auto- und Möbelleder, Schweiß durch Füße in Schuhen (täglich zwischen 100-200 ml), Hände in Handschuhen oder "Speckkragen" bei Jacken).
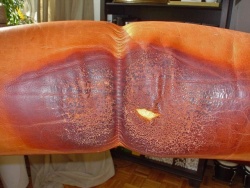
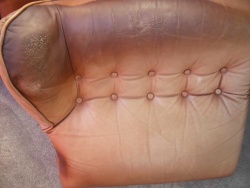
Typische Schäden durch Haut- und Haarkontakt bei Möbelledern (Kopfteile und Armlehnen).
Auch Lenkräder reagieren mit der Zeit auf Handschweiß. Durch die pH-Verschiebung wird das Leder auch anfälliger für Schimmelbefall.
Durch Hautkontakt geschädigte Auto-Armlehnen und ein Schaltknauf.
Ein weiterer Grund sind alkalische Reiniger. Die meisten Haushaltsreiniger sind alkalisch, weil dann problemlos eine gute Reinigungswirkung entsteht. Lederreiniger sollten aber nicht alkalisch sein, was technisch auch möglich ist, aber nicht von allen Herstellern beachtet wird.
Auch die Pflegemittel sollten idealerweise den sauren Zustand wiederherstellen bzw. aufrechterhalten. Gerade bei [[Schimmel|Schimmelbefall] an Altledern eignet sich beispielsweise Essigessenz als pH-Regulator zur Entfernung und Vorbeugung vorzüglich. Auch bei der generellen Altlederrestauration ist eine Rücksäuerung ebenso wichtig wie eine Rückfettung, um das Leder wieder resistenter gegen Umwelteinflüsse zu machen.
Gleichwohl gibt es natürlich auch eine Grenze, wieviel Säure ein Leder verträgt. Ein gelegentlich in Bibliotheken zu beobachtender, charakteristischer Säureschaden an Bucheinbänden ist etwa der Rote Zerfall, wenn Schwefeldioxid aus der Luft im Leder zu Schwefelsäure reagiert, die den Einband irreparabel zerfrisst. Schwefelsäure ist allerdings auch eine der stärksten Säuren und untertrifft den für Leder maximal verträglichen pH-Wert von 3,5 bei weitem.
| Substanz | pH-Wert | Art |
|---|---|---|
| Batteriesäure | <0 | ↓ |
| Magensäure (nüchterner Magen) | 1,0–1,5 | sauer |
| Zitronensaft | 2,4 | |
| Cola | 2–3 | |
| Fruchtsaft der Schattenmorelle | 2,7 | |
| Essig | 2,9 | |
| Orangen- und Apfelsaft | 3,5 | |
| Wein | 4,0 | |
| Saure Milch | 4,5 | |
| Bier | 4,5–5,0 | |
| Saurer Regen | < 5,0 | |
| Kaffee | 5,0 | |
| Tee | 5,5 | |
| Regen (natürlicher Niederschlag) | 5,6 | |
| Mineralwasser | 6,0 | |
| Milch | 6,5 | |
| Wasser (je nach Härte) | 6,0–8,5 | |
| NEUTRAL | 7,0 | |
| Menschlicher Speichel | 6,5–7,4 | |
| Blut | 7,4 | basisch |
| Meerwasser | 7,5–8,4 | |
| Pankreassaft (Darmsaft) | 8,3 | |
| Seife | 9,0–10,0 | |
| Haushalts-Ammoniak | 11,5 | |
| Bleichmittel | 12,5 | |
| Beton | 12,6 | |
| Natriumhydroxid, Natronlauge (Ätznatron) | 13,5–15 |
Weitere Informationen















 a kotori web solution
a kotori web solution